

文獻題目:A male-pheromone-elevated transcription factor ZNF362.1 in female schistosomes determines sexual maturation
發表期刊:Science Advances
影響因子:12.5
發表時間:2026年3月6日
發表單位:復旦大學
藍景科信提供:DAP-seq技術服務
主要研究內容
血吸蟲病由血吸蟲感染所致,全球受影響人群超2億,雌性血吸蟲的產卵行為是該病傳播和病理損傷發生的關鍵環節。已知雌性血吸蟲的卵巢與卵黃腺成熟依賴雄性分泌的信息素β-丙氨酰-色胺(BATT),但BATT觸發雌性生殖成熟的下游分子調控通路此前尚未明確。
本研究解析了BATT調控雌性生殖成熟的分子機制,發現轉錄因子znf362的長異構體znf362.1是BATT誘導雌性卵巢和卵黃腺成熟的下游關鍵調控因子,該因子在BATT處理后,于卵巢卵母細胞和卵黃腺S1細胞中特異性上調,且僅調控生殖干細胞的分化過程,不影響其增殖。
研究團隊通過DAP-seq技術繪制了ZNF362.1的全基因組結合圖譜,發現其DNA結合域優先結合基因組的內含子(40.56%)和遠端基因間區(37.80%),僅有9.65%的結合峰位于啟動子區域;同時鑒定出六核苷酸“AAAAAA"為其富集度最高的特異性結合基序。接著通過DAP-seq與RNA-seq聯合分析,篩選出其直接靶基因為Smp_349410。經EMSA、Dual-LUC等進一步驗證,ZNF362.1可通過結合Smp_349410的啟動子直接激活其轉錄,而該基因編碼的SmCPEB1通過差異化機制調控生殖器官成熟:在卵巢中,通過調控cyclin B1 mRNA的多聚腺苷酸化促進卵母細胞減數分裂;在卵黃腺中,則通過不依賴cyclin B1的通路驅動S1細胞分化。
本研究由此系統闡明了“BATT-ZNF362.1-cpeb1"信號軸調控雌蟲性成熟的分子機制,并揭示了CPEB1在卵巢與卵黃腺中的差異化調控路徑。這一發現為理解血吸蟲的生殖調控機制提供了全新視角,也為研發阻斷蟲卵傳播的血吸蟲病干預策略提供了重要的理論支撐與潛在分子靶點。
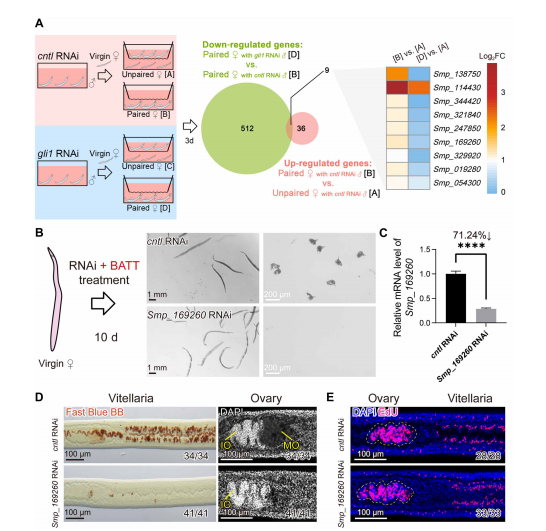
圖1. BATT誘導的znf362調控未交配雌性血吸蟲的性成熟過程。(A)RNA-seq分析顯示,未交配雌蟲中有9個基因在交配后第3天受雄性信息素誘導表達上調。[B]與[A]比較用于鑒定與可產生BATT的對照雄蟲配對后,未交配雌蟲中表達上調的基因;與之相對,[D]與[A]比較則揭示了與BATT缺陷型雄蟲(gli1敲低雄蟲,喪失BATT合成能力)配對后,未交配雌蟲中上調的基因。n=3。(B)光學顯微鏡觀察未交配雌蟲在體外經對照組或Smp_169260-RNAi處理10天后的形態學特征及產卵情況。左圖:dsRNA處理流程示意圖;中圖:蟲體整體形態(標尺,1 mm);右圖:蟲卵形態(標尺,200 μm)。n=3。(C)RNAi處理10天后未交配雌蟲中Smp_169260敲除的qPCR檢測結果。n=3。數據以平均值±標準差(mean±SD)表示,****P<0.0001。(D)經對照或Smp_169260-RNAi處理10天后,未交配雌蟲卵黃腺和卵巢Fast Blue BB及DAPI染色結果。成熟卵黃腺經Fast Blue BB染色呈紅棕色(左圖)。在卵巢中(右圖),未成熟卵母細胞(IO)表現為染色質致密、DAPI強熒光區域,而成熟卵母細胞(MO)染色較淺且細胞體積更大。n=3。標尺,100 μm。(E)經對照組或Smp_169260dsRNA處理7天后,卵巢及卵黃腺中增殖細胞的EdU標記情況。EdU陽性細胞呈品紅色,細胞核用DAPI復染呈藍色。卵巢區域用黃色虛線標注。n=3。標尺,100 μm。(C) 采用獨立樣本Student’st檢驗。
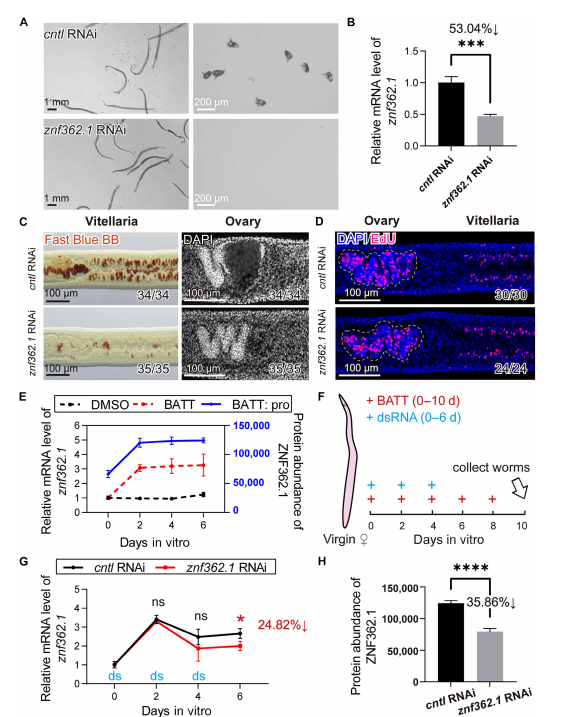
圖2. 最長轉錄本亞型znf362.1對未交配雌性血吸蟲的生殖發育至關重要。(A)光學顯微鏡觀察經對照組或znf362.1 dsRNA體外處理10天后未交配雌蟲的形態學特征及產卵情況。n=3。比例尺:蟲體整體形態1 mm;蟲卵形態200 μm。(B)RNAi處理10天后znf362.1敲除的qPCR檢測結果n=3。數據以平均值±標準差表示。***P<0.001。(C)經對照組與znf362.1-RNAi處理10天后,未交配雌蟲卵黃腺和卵巢的Fast Blue BB與DAPI染色結果。卵黃腺Fast Blue BB染色(左圖);右側為卵巢DAPI染色(右圖)。n=3。比例尺100 μm。(D)經對照組與znf362.1 dsRNA處理7天后,卵巢和卵黃腺中增殖細胞的EdU標記情況。EdU陽性細胞呈品紅色,細胞核經DAPI復染呈藍色。卵巢區域用黃色虛線標注。n=3。比例尺100 μm。(E)BATT誘導后D0至D6期間znf362.1轉錄和蛋白水平定量分析。黑色和紅色虛線代表轉錄水平,藍色實線代表蛋白豐度。n=3~4。數據以平均值±標準差表示。(F)雌蟲6天RNAi處理實驗設計示意圖。(G)對照組與RNAi處理組D0至D6期間znf362.1轉錄水平qPCR定量結果(*P=0.03)。n=3。數據以平均值±標準差表示。(H)通過基于DIA的定量蛋白質組學分析測定的對照組與znf362.1-RNAi組在D6時間點的ZNF362.1蛋白豐度(****P<0.0001)。n=4。數據以平均值±標準差表示。(B)、(E)、(G)和(H)均采用非配對Student’s t檢驗。
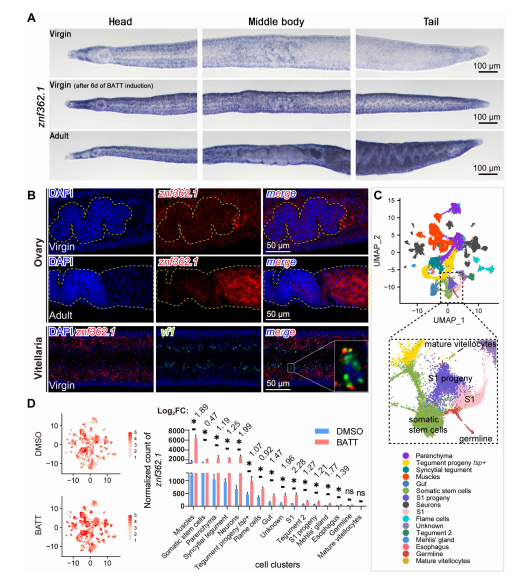
圖3. znf362.1基因表達譜及其響應BATT刺激的單細胞動態變化。(A) WISH顯示未交配雌蟲、在A169培養基中經BATT誘導6天的未交配雌蟲及成蟲雌蟲中znf362.1的表達情況。紫色染色標記mRNA定位。比例尺100 μm。圖像具有代表性,n>12條蟲體,來自3次生物學重復。(B)FISH顯示未交配雌蟲卵巢與卵黃腺、成蟲雌蟲卵巢中znf362.1的表達情況。比例尺50 μm。圖像具有代表性,n>12條蟲體,來自3次生物學重復。(C)基于已鑒定的細胞類型標記基因對未交配雌蟲scRNA-seq數據進行聚類分析的UMAP圖。(D)對照組與BATT處理組中znf362.1表達的單細胞分辨率分析。左圖:UMAP圖展示znf362.1的相對表達水平,紅色表示表達量更高;右圖:第2天對照組與BATT處理組間不同細胞類型中znf362.1表達量的定量比較。n=3。數據以平均值±標準差表示(*P.adj<0.05)。
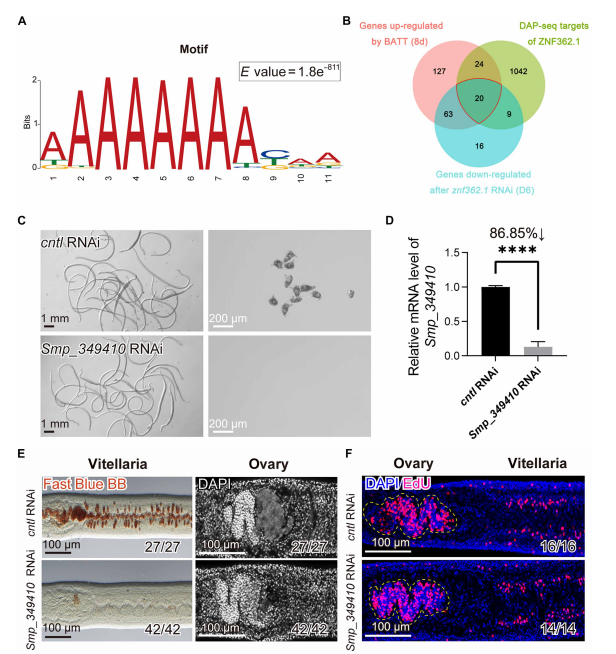
圖4. Smp_349410作為ZNF362.1的潛在下游靶標參與雌蟲性成熟過程。(A)基于DAP-seq結果預測的ZNF362.1結合概率最高的DNA結合基序。(B)韋恩圖展示三組基因的交集:BATT處理8天后表達上調的基因、znf362.1 RNAi處理6天后表達下調的基因,以及經DAP-seq鑒定的、啟動子區域可被ZNF362.1 DNA結合結構域(DBD)結合的基因。(C)經對照組或Smp_349410 dsRNA處理21天(自第7天開始BATT誘導)后,光學顯微鏡觀察未交配雌蟲的形態學特征及產卵情況。n=3。比例尺:蟲體整體形態1 mm;蟲卵形態200 μm。(D)RNAi處理21天(自第7天開始BATT誘導)后未交配雌蟲中Smp_349410敲低的qPCR檢測結果。n=3。數據以均值±標準差表示。****P<0.0001。(E)經對照組與Smp_349410-RNAi處理21天(自第7天開始BATT誘導)后未交配雌蟲卵黃腺和卵巢的Fast Blue BB與DAPI染色結果。卵黃腺Fast Blue BB染色(左圖);卵巢DAPI染色(右圖)。n=3。比例尺100 μm。(F)經對照組或Smp_349410 dsRNA處理7天后,卵巢和卵黃腺中增殖細胞的EdU標記情況。EdU陽性細胞呈品紅色,細胞核經DAPI復染呈藍色。卵巢區域用黃色虛線標注。n=3。比例尺100 μm。(D)采用非配對Student’s t檢驗。
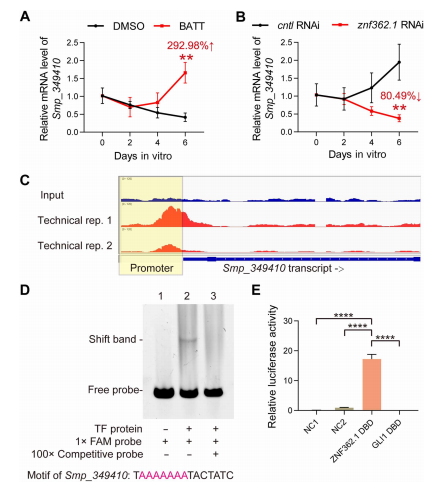
圖5. Smp_349410是血吸蟲ZNF362.1的直接轉錄靶基因。(A)qPCR定量檢測對照組與BATT誘導條件下,未交配雌蟲D0~D6 Smp_349410的轉錄水平。n=3。數據以平均值±標準差表示。**P<0.01。(B)BATT誘導條件下,qPCR定量檢測對照組與Smp_349410-RNAi組未交配雌蟲0~6天Smp_349410的轉錄水平。n=3。數據以平均值±標準差表示。**P<0.01。(C)IGV展示DAP-seq在Smp_349410基因位點的覆蓋度。軌跡圖展示了兩個技術重復及一個input對照樣本中,比對至曼氏血吸蟲參考基因組(版本10)的reads。y軸表示單堿基reads覆蓋度。啟動子區域以黃色方框標注。(D)EMSA驗證ZNF362.1與Smp_349410啟動子基序的結合。泳道1:僅FAM標記探針(無蛋白);泳道2:FAM標記探針與ZNF362.1 DBD共孵育;泳道3:加入100倍摩爾過量的未標記探針進行競爭結合。(E)雙熒光素酶報告基因實驗驗證ZNF362.1 DBD對Smp_349410啟動子的轉錄激活作用。NC1(陰性對照1):空載pcDNA3.1載體+含Smp_349410啟動子的報告質粒;NC2(陰性對照2):ZNF362.1 DBD表達質粒+不含Smp_349410啟動子的報告質粒;ZNF362.1 DBD:含Smp_349410啟動子的ZNF362.1 DBD-VP64-NLS表達質粒+報告質粒。GLI1 DBD:GLI1 DBD-VP64-NLS表達質粒+含Smp_349410啟動子的報告基因載體。n=3。數據以均值±標準差表示。****P<0.0001。(A)、(B)和(E)采用非配對Student‘s t檢驗。

圖6. Smp_349410在雌性血吸蟲生殖腺中特異性表達。(A)WISH顯示Smp_349410 在未交配雌蟲、在A169中經BATT處理6天的未交配雌蟲及成蟲雌蟲中的表達情況。紫色染色標記mRNA定位。比例尺100 μm。代表性圖像來自3次生物學重復,n>12條蟲體。(B)FISH顯示Smp_349410在未交配雌蟲卵巢及卵黃腺、成蟲雌蟲卵巢中的表達情況。比例尺50 μm。代表性圖像來自3次生物學重復,n>12條蟲體。(C)對照組與BATT處理組中Smp_349410表達的單細胞分辨率分析。左圖:UMAP圖展示Smp_349410的平均表達水平,紅色表示表達量更高;右圖:D2對照組與BATT處理組間不同細胞類型中Smp_349410表達量的定量比較。n=3。數據以平均值±標準差表示(*P.adj<0.05)。(D)基于已鑒定的細胞類型標記基因對成年雌蟲生殖系scRNA-seq數據進行聚類分析的UMAP圖。(E)成年雌蟲生殖系中Smp_349410表達的UMAP圖,紅色表示表達水平更高。
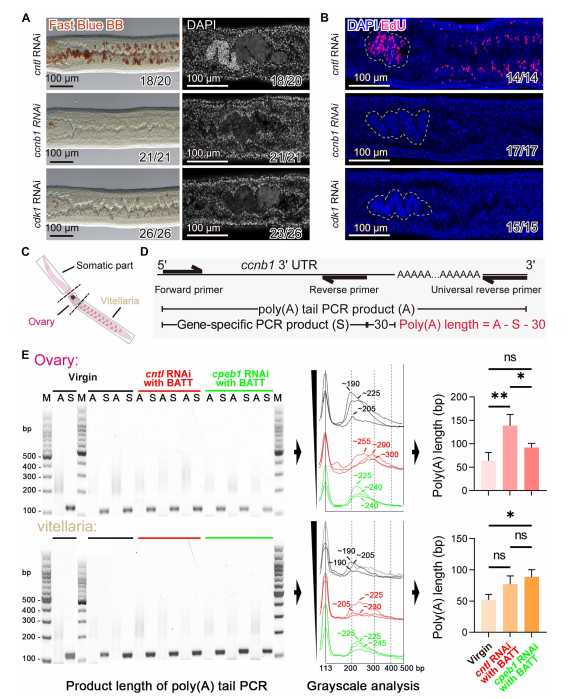
圖7. Cpeb1在雌性血吸蟲生殖發育過程中調控cyclin B1 mRNA多聚腺苷酸化。(A)經對照組、ccnb1或cdk1 dsRNA處理19天后(自D7開始BATT誘導),雌蟲卵黃腺和卵巢的Fast Blue BB和DAPI染色結果。卵黃腺Fast Blue BB染色(左圖);卵巢DAPI染色(右圖)。n=3。比例尺:100 μm。(B)經對照組、ccnb1或cdk1 dsRNA處理7天后,卵巢和卵黃腺中增殖細胞的EdU標記情況。EdU陽性細胞呈品紅色;細胞核經DAPI(藍色)復染。卵巢區域用黃色虛線標出。n=3。比例尺:100 μm。(C)用于RNA提取的體組織、卵巢及卵黃腺解剖示意圖;方框區域為從雌蟲中切取的組織部位。(D)基于PCR分析cyclin B1 mRNA多聚腺苷酸尾(poly(A))長度的實驗示意圖。Poly(A)PCR擴增poly(A)區域(A);基因特異性PCR靶向3'UTR區域(S)用于比對。尾長計算公式為A?S?30[S=113 bp;30為反向引物至poly(A)起始位點的距離]。(E)未交配雌蟲、BATT誘導對照RNAi雌蟲及BATT誘導cpeb1 RNAi雌蟲的體組織、卵巢和卵黃腺中cyclin B1 mRNA的poly(A)尾分析。A:poly(A)尾PCR產物;S:基因特異性PCR產物;M:100 bpDNA分子量標準。經灰度分析后根據峰頂點(箭頭)估算相對poly(A)尾長度。n=3。數據以平均值±標準差表示。**P<0.01,*P<0.05。(E)采用非配對Student’s t 檢驗。
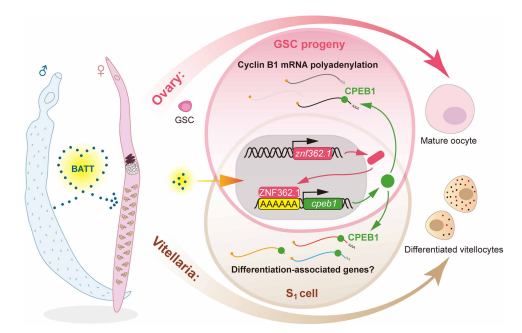
圖8. ZNF362.1介導曼氏雌性血吸蟲響應雄蟲來源BATT信號調控性發育的轉錄調控模式圖。在未交配雌蟲中,卵巢與卵黃腺的分化處于停滯狀態,卵巢發育阻滯于生殖干細胞(GSC)子代階段,卵黃腺發育阻滯于S1細胞階段。雌雄配對后,雄蟲來源的信息素BATT誘導雌蟲中轉錄因子znf362.1表達上調。ZNF362.1隨后在卵巢和卵黃腺中均激活cpeb1的轉錄。在卵巢中,CPEB1水平升高可增強減數分裂關鍵調控因子cyclin B1 mRNA的多聚腺苷酸化,進而促進卵母細胞成熟。在卵黃腺中,CPEB1通過一條似乎不依賴cyclin B1 mRNA多聚腺苷酸化的通路調控增殖態S1細胞的分化進程。
